编者按:随着研发技术的不断进步,新一代共价药物的开发已成为业界高度关注的方向。截至目前,已有超过50种共价药物成功获批上市,并在多个疾病领域展现出显著疗效。值得关注的是,新一代共价药物正不断突破局限,向可逆性共价结合及靶向半胱氨酸以外氨基酸残基的方向快速拓展,为攻克“不可成药”靶点带来全新契机。依托端到端的CRDMO赋能平台,药明康德致力为全球合作伙伴提供覆盖共价药物发现与开发的一体化解决方案。本文将回顾2025年第三季度共价小分子领域的最新进展,并介绍药明康德在共价药物发现领域的技术与能力。
共价抑制剂在癌症领域持续进展
自KRAS G12C抑制剂sotorasib与adagrasib获批以来,共价小分子在攻克癌症领域“不可成药”靶点方面的潜力,愈发受到产业界的广泛关注。进入2025年第三季度,多款KRAS G12C共价抑制剂陆续获得美国FDA授予的突破性疗法认定(BTD),用于治疗非小细胞肺癌(NSCLC),其中包括olomorasib、RAS(ON)G12C选择性抑制剂elironrasib(RMC-6291),以及RAS(OFF)G12C选择性抑制剂D3S-001。RAS(ON)与RAS(OFF)分别指RAS分子处于活性与非活性状态。值得一提的是,先前公布的研究结果显示,在36例既往接受免疫治疗与化疗的KRAS G12C突变NSCLC患者中,elironrasib治疗组的客观缓解率(ORR)达到56%,疾病控制率(DCR)高达94%。
除KRAS G12C外,针对KRAS G12D的共价抑制剂研发也在快速推进。其中,RAS(ON)G12D选择性抑制剂zoldonrasib(RMC-9805)的临床前研究成果于今年7月发表在《科学》杂志上。目前,该疗法已进入临床阶段。根据已公布的数据,在18例可评估疗效、携带KRAS G12D突变的经治NSCLC患者中,ORR达到61%,DCR为89%。
除KRAS外,其他靶点的共价抑制剂研发也持续进展。例如,评估潜在“best-in-class”口服共价Werner解旋酶抑制剂MOMA-341的1期临床试验已完成首例患者给药。该研究旨在治疗具有高微卫星不稳定性(MSI-H)和/或DNA错配修复缺陷(dMMR)的晚期或转移性实体瘤,包括结直肠癌、胃癌和子宫内膜癌等。
其他适应症的应用拓展
除了肿瘤领域,共价抑制剂的应用也正在向免疫、代谢及炎症性疾病拓展。
今年8月,美国FDA批准赛诺菲(Sanofi)共价抑制剂Wayrilz(rilzabrutinib)上市,用于治疗既往疗效不足的持续性或慢性免疫性血小板减少症(ITP)成人患者。根据新闻稿,Wayrilz是FDA批准的首款用于ITP治疗的布鲁顿氏酪氨酸激酶(BTK)抑制剂。3期临床数据显示,第25周时,Wayrilz组23%的患者达到持久性血小板应答,而安慰剂组为0%(p<0.0001)。此外,Wayrilz组患者的血小板应答持续时间显著延长至7周,而安慰剂组仅为0.7周。同月,Wayrilz还获得欧洲药品管理局(EMA)授予孤儿药资格,用于治疗IgG4相关疾病。
在皮肤疾病领域,ITK与JAK3双靶点抑制剂ATI-2138在治疗中重度特应性皮炎(AD)的2a期试验中达到了主要及关键次要终点。研究结果显示,该药疗效与活性对照药物相当,并展现出良好的安全性。研发方计划进一步评估其在斑秃及其他作用机制相似疾病中的潜在疗效。
代谢疾病领域同样出现新的探索。用于治疗2型糖尿病(T2D)的menin靶向共价抑制剂icovamenib在公布的动物实验结果显示,与GLP-1受体激动剂(GLP-1RA)联用可更有效地控制血糖并减轻体重,同时保持瘦体重,其疗效优于GLP-1RA单药。该疗法目前正在多项2期试验中评估,用于单药或联合GLP-1RA治疗T2D患者。
商业合作进展
共价药物领域的活跃也体现在产业合作与融资上。
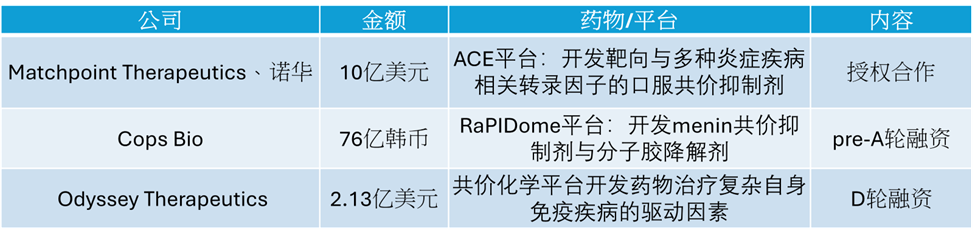
今年7月,诺华(Novartis)与Matchpoint Therapeutics达成最高金额约10亿美元的独家选择权与许可协议,双方将合作开发和商业化一款口服共价抑制剂,该药物靶向一类与多种炎症性疾病相关的转录因子。根据协议,Matchpoint将利用其Advanced Covalent Exploration(ACE)平台推进前期研究,直至筛选出候选化合物。
此外,Odyssey Therapeutics也在今年9月完成2.13亿美元融资,旨在通过其人工智能与共价化学平台加速开发用于治疗自身免疫疾病的新药。
▲部分2025年第三季度共价小分子疗法相关合作交易与融资事件
总体来看,共价抑制剂正从肿瘤领域不断向免疫、炎症与代谢等多类疾病扩展,其独特的结合机制、持久效率与高选择性特征,正在为多种疾病带来新的解决方案。随着技术平台的成熟与产业合作的加深,这一领域有望在未来几年迎来更多临床与商业化突破。
药明康德助力加速共价药物开发
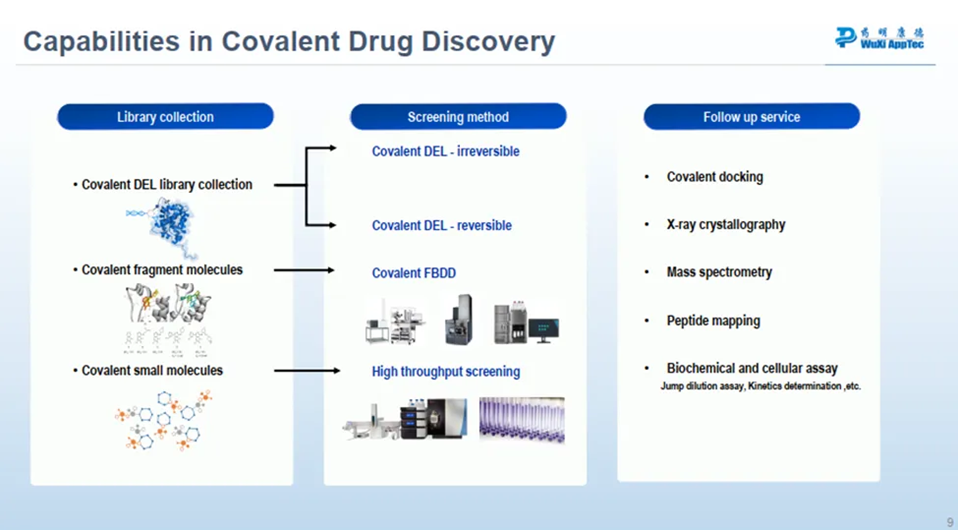
为帮助全球合作伙伴加速下一代共价药物的研发——从早期发现到IND申报,药明康德建立了一体化发现平台。该平台融合了三大互补技术:共价DNA编码化合物库(cDEL)、共价片段药物发现(cFBDD)以及共价高通量筛选(cHTS),为共价药物发现提供了高效的解决方案。
▲药明康德共价药物发现能力
cDEL是一项功能强大的筛选技术,能够高效探索庞大的化学空间,大幅提升发现多样化共价分子及其结合弹头的可能性。通过将DNA标签作为“分子条形码”,该平台可在仅需极少量蛋白和化合物的条件下,实现快速且具成本效益的苗头化合物发现,在化学多样性至关重要的早期研发阶段尤为突出。
药明康德的cFBDD平台则基于一个经过严格筛选的化合物库,包含超过2600个结构多样化的片段。该平台以小而低复杂度的分子片段为核心,高效探索结合位点,并通过引入带有亲电基团的片段,快速识别可作为优化起点的共价结合物。结合高通量质谱以及X射线晶体学、核磁共振(NMR)等结构生物学方法,cFBDD能够在原子水平提供片段–蛋白相互作用的深度洞察,从而支持理性设计与系统优化。
药明康德的cHTS平台是集合了药明康德cHTS共价库和多种筛选方法的高通量筛选平台。药明康德的cHTS共价库约有6万9千个分子,涵盖50多种不同类型的共价弹头,反应活性范围多样。这些化合物能够作用于九类不同的氨基酸残基,将共价药物发现的范围从半胱氨酸扩展至丝氨酸、赖氨酸以及其他残基专属的化合物库。
在共价药物筛选平台之外,药明康德还建立了一整套早期药物发现技术平台,涵盖生物物理学、生物化学及细胞学检测,为全球合作伙伴共价药物的开发提供坚实的支持。依托端到端的一体化CRDMO赋能平台,药明康德致力于加速突破性疗法的开发,帮助合作伙伴将创新成果高效转化为造福全球患者的解决方案,以践行“让天下没有难做的药,难治的病”的愿景。
配资客户提示:文章来自网络,不代表本站观点。